+ 86-19102685862
- 全部
- 产品名称
- 关键词
- 产品型号
- 产品摘要
- 产品描述
- 全文搜索
- 全部
- 产品名称
- 关键词
- 产品型号
- 产品摘要
- 产品描述
- 全文搜索

关于生物药物修饰物研究指导原则的解读
药物的半衰期决定了它在体内的停留时间,药物半衰期过短可以通过缩短给药间隔和增加给药剂量来补偿,但存在成本和安全性以及依从性方面的限制。那些获得了监管批准的多肽药物与内源性肽相比,药物的血浆半衰期显著提高,为我们提供了将肽的体内稳定性从几分钟提高到几小时或更长时间的成功案例。多肽类药物使用不同的化学结构修饰策略,延缓血液或组织蛋白酶介导的降解和失活,从而增强多肽候选药的成药性。
2022年4月,CDE发布《胰岛素类产品生物类似药药学研究与评价技术指导原则》。虽然该指南明确的适用范围为采用重组产品技术表达、制备的7种胰岛素类产品的生物类似药,实际上现代药品研发与生产本质应基于科学性(数据)和风险管理,旨在保证药品的安全性和有效性,因此对于其他重组表达的肽类药品的生物类似药均可参考本指导原则。
笔者认为,采用化学合成的多肽,虽然在肽链的制备工艺路线与上重组类的生物类似物不同,但其侧链修饰砌块的本质是一样的,因此可在一定程度上酌情参考本指导原则。
指导原则中对小分子修饰物的表述如下:
(一)起始原材料
2. 小分子修饰物
小分子修饰物是改变胰岛素类产品药代动力学行为的重要因素之一,可根据其结构特征及制备工艺,充分评估其质量对产品安全性、有效性和质量可控性的潜在影响,重点关注其杂质控制能力,如降解产物、异构体、遗传毒性杂质、有机溶剂和元素杂质等。尽早确定小分子修饰物的制备工艺或供应商,确保批间质量一致以及临床试验样品的代表性。
2.1 生产工艺
若自行生产小分子修饰物,其制备用起始原材料的选择应参考 ICH Q11 和相关技术要求,建立合理的内控标准;对关键的工艺中间体拟定合理的控制标准。
2.2 结构确证
可参考《化学药物原料药制备和结构确证研究的技术指导原则》等的要求,结合工艺路线,采用多种分析测试方法对小分子修饰物化学结构进行结构研究,对含有立体构型的小分子修饰物,可采用单晶 X 衍射、核磁共振等手段进行立体结构的确证研究。
2.3 质量标准
根据胰岛素类产品质量控制要求,结合小分子修饰物制备工艺,合理拟定小分子修饰物质量标准的控制项目、方法和限度。对于潜在的、具有遗传毒性的杂质可按照 ICH M7的要求进行风险评估和控制。
2.4 稳定性
应参照 ICH Q1A(R2)、Q1B 和《化学药物(原料药和制剂)稳定性研究技术指导原则》进行相关研究,拟定合理的贮藏条件和复验期。
指南对小分子修饰物工艺研究和质量控制均给出了具体的要求,其涵盖的内容包含如下方面:
• 结合本指南和《化学合成多肽药物药学研究技术指导原则(试行)》,无论是重组表达还是化学合成多肽,都可以考虑将小分子修饰物定义为起始物料。当然,从与监管机构交流及经验的角度出发,将小分子修饰物定义为起始物料还是GMP中间体,本质上还需企业基于风险管理和质量控制的角度予以考量,应重点关注修饰物结构与工艺的复杂程度、修饰物质量的可控性、修饰物的CMA与药品CQA的联系。
• 监管上实际上对小分子修饰物的研究和控制提出的要求高于起始物料,而更倾向于贴近原料药的管理。小分子修饰物的研发与生产,应照ICH Q11的要求选择适宜的起始原料,拟定合理的合成路线。依据杂质的来源、清除能力、质量风险的考虑,从原料引入、过程产生(副反应、残留物料或中间体及其跳步反应物)、降解杂质等角度充分评估潜在杂质,并制定原料、中控、中间体等各阶段的控制策略。小分子修饰物在与肽链缩合后,还需要经历一系列的后续化学反应,杂质限度的建立还应充分考虑后续药品生产工艺对其的清除或富集能力,针对不同的杂质进行分类控制(如高毒性杂质、可偶联杂质、不可偶联杂质、后续工艺中还会使用和不再使用的溶剂等),既要保证药品的安全性和有效性,也可以避免过度控制造成的无效成本增加。
• 小分子修饰物对多肽药品药代动力学具有重要意义,随着研究推进至一定阶段,若要变更供应商,风险等级较高,应进行充分的评估和研究,不排除可能重新进行包含药代动力学的非临床或临床研究。应尽早确定供应商,这其实为研发阶段对供应商的选择提出了更高的要求,即在研究的早期阶段就应考虑拟选择的供应商是否能够满足临床后期和商业批的质量和产能需求。
成都普康专注于多肽侧链修饰物的研发与生产,公司的司美格鲁肽系列侧链修饰剂均参考原料药的研究要求进行药学研究,对杂质谱进行了详细评估和控制,必要时可配合客户进行后续使用修饰剂工艺的杂质去除验证,以制定更合理的修饰剂质量标准,并参照ICH M4的要求撰写DMF文件,目前公司的司美格鲁肽系列侧链修饰剂主要品种均已完成DMF文件,其中部分已申报(FDA备案或国内客户作为附件申报CDE)。公司生产基地参照GMP和ICH Q7建立质量管理体系,目前该系列主要品种均在工厂完成工艺验证,并且具有足够的产能满足客户药品商业化需要。
成都普康司美格鲁肽系列产品
司美系列 | 产品名称&CAS | 产品结构 | 是否完成药学研究 | 批量 |
重组发酵用侧链 | tBuO-Ste-Glu(AEEA-AEEA-OH)-OtBu CAS:1118767-16-0 | | 是,DMF已作为附件申报CDE | 40kg/批 |
tBuO-Ste-Glu(OtBu)-AEEA-AEEA-OSU CAS:1118767-15-9 | | 在研,进行至成品方法学研究 | 10kg/批 | |
Ste-Glu-AEEA-AEEA-OSU CAS:1169630-40-3 |
| 是,DMF已作为附件申报CDE | 10kg/批 | |
固相合成用侧链 | Fmoc-L-Lys[Oct-(OtBu)-Glu-(OtBu)-AEEA-AEEA]-OH CAS:1662688-20-1 |
| 是,DMF文件已进入翻译阶段,拟在FDA备案 | 40kg/批 |
成都普康将同系物杂质、缺失和错结肽、异构体杂质等可偶联杂质作为重要的杂质进行控
制tBuO-Ste-Glu(AEEA-AEEA-OH)-OtBu(CAS:1118767-16-0)
有关物质系统适用性图谱:
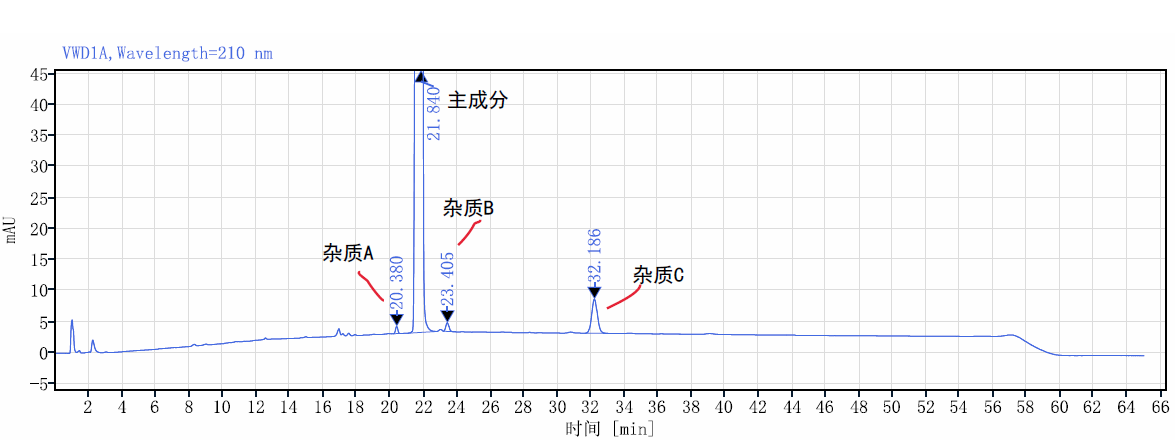
异构体系统适用性图谱:
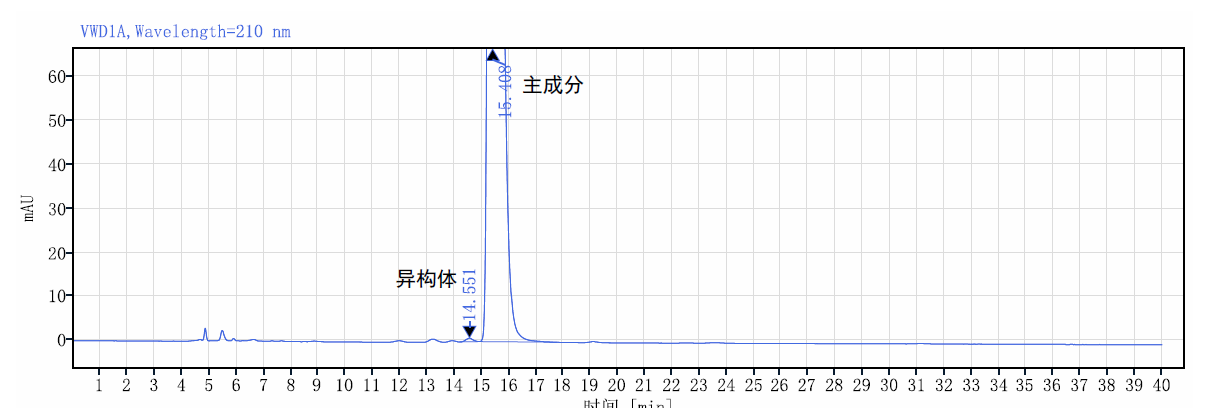
Ste-Glu-AEEA-AEEA-OSU(CAS:1169630-40-3)
有关物质1,有关物质2系统适用性图谱:
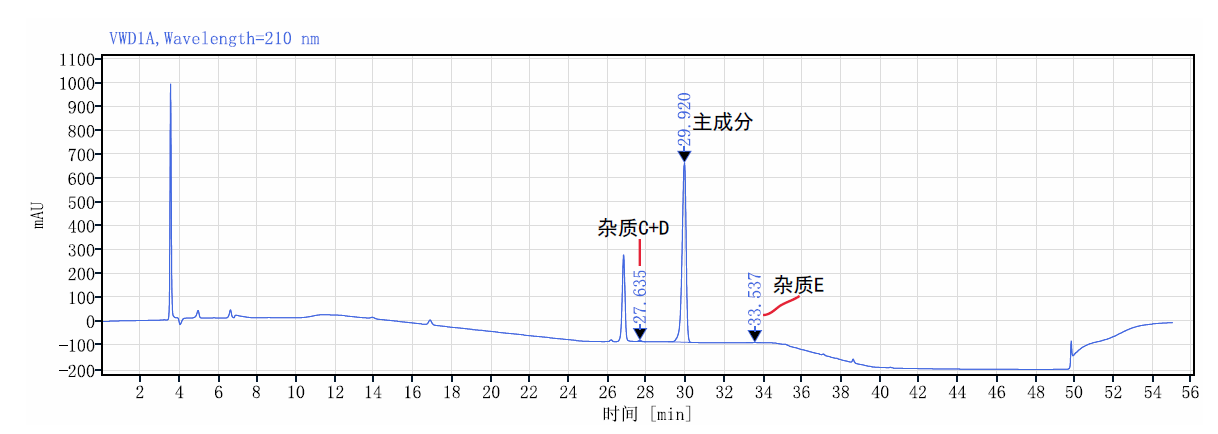
有关物质1
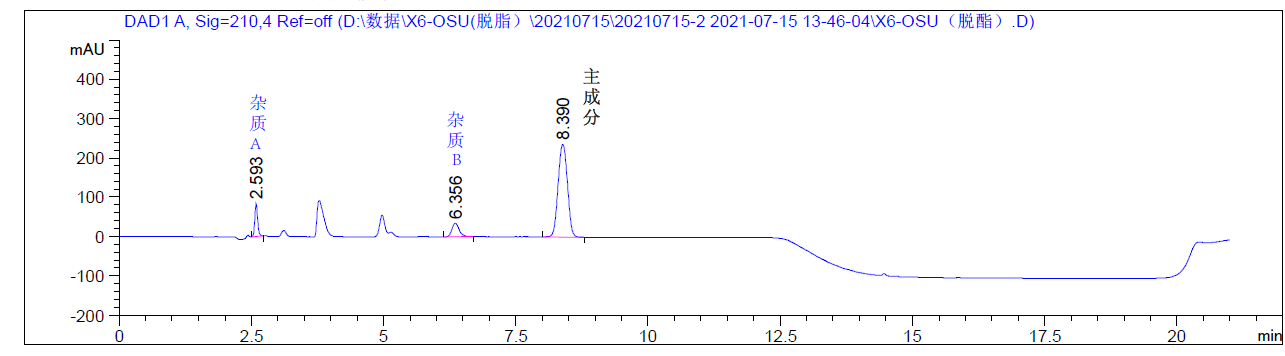
有关物质2
Fmoc-L-Lys[Oct-(OtBu)-Glu-(OtBu)-AEEA-AEEA]-OH(CAS:1662688-20-1)
有关物质系统适用性图谱:
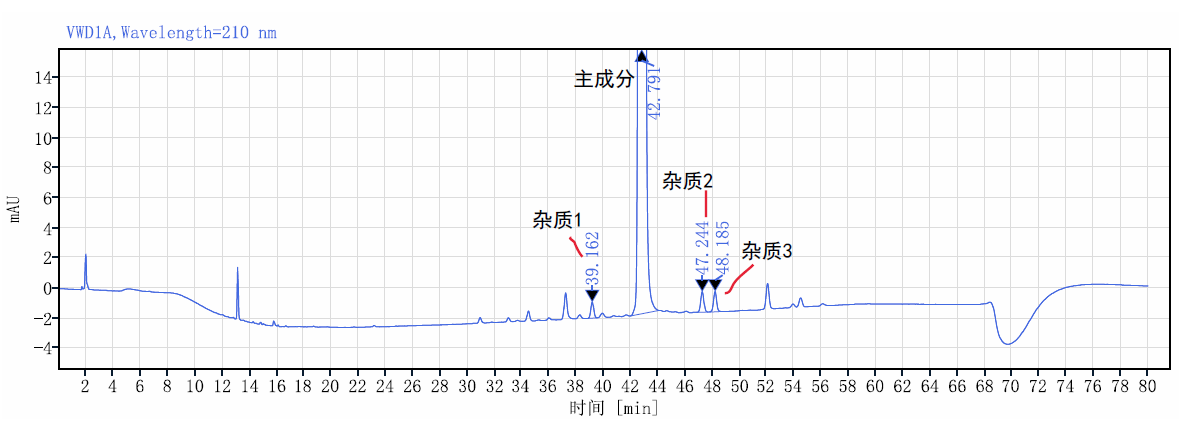
异构体系统适用性图谱:
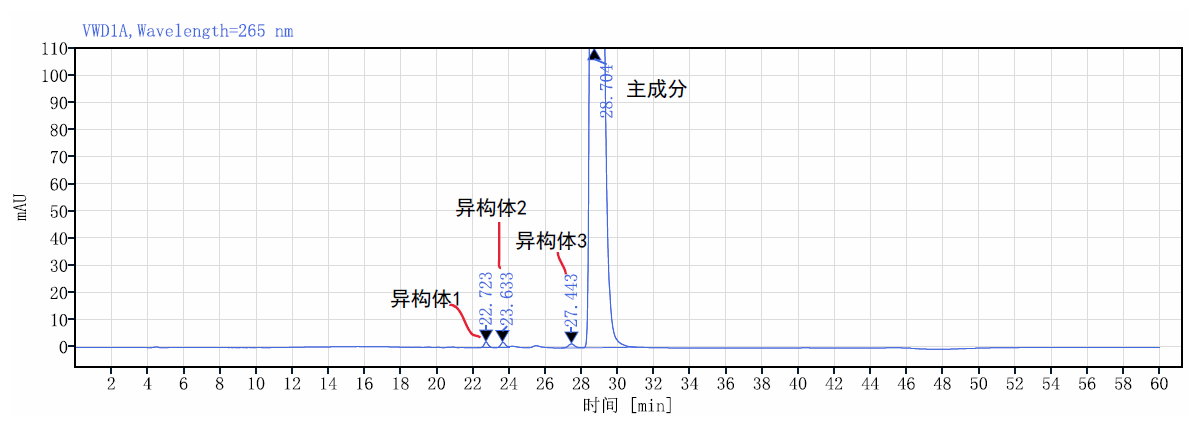
多肽侧链的批产量及批间稳定性对API的质量控制非常重要。为满足客户的商业化批量需求,我司建立的生产基地四川普康药业有限公司于2023年5月正式运行,总占地面积103.4亩,一期建设用地48亩,建筑面积15000平方米,建有三条生产线,38个多功能反应釜及系列中试设备,全方位满足客户的产业化需求。


公司秉承“质量为上,创新先行,以人为本,诚信为根”的经营理念,为全球多肽企业提供优质稳定的多肽长效化侧链品种!