+ 86-19102685862
- 全部
- 产品名称
- 关键词
- 产品型号
- 产品摘要
- 产品描述
- 全文搜索
- 全部
- 产品名称
- 关键词
- 产品型号
- 产品摘要
- 产品描述
- 全文搜索

1.1 向阳花木易为春,小核酸药物优势显著
讲到堪称生物医药第三次革命的核酸药物就不得不提到中心法则。中心法则是指 遗传信息从 DNA 传递给 RNA,再从 RNA 传递给蛋白质的转录和翻译的过程,以及 遗传信息从 DNA 传递给 DNA 的复制过程。这是所有有细胞结构的生物所遵循的法 则。核酸药物就是有别于传统药物,直接作用在 DNA 或者 RNA 层面的药物,本报 告重点分析在核酸药物中碱基较少(往往小于 30nt)的小核酸药物。
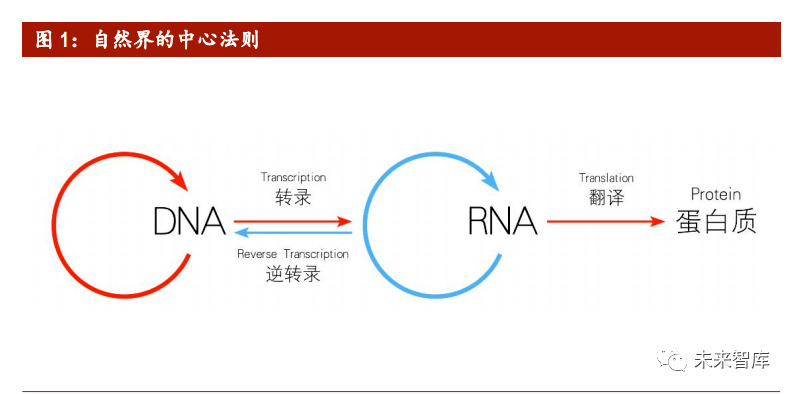
基于 RNA 和 DNA 的核酸药物较之传统药物更有优势。目前,小分子和蛋白质是生 物制药主流的两大类药物。小分子药物通过竞争性结合抑制靶蛋白,而基于蛋白 质的药物(例如抗体)可以与多个靶标高度特异性结合。相较于抗体药物,小核 酸药物可选择靶点更为丰富,特别是针对一些蛋白药物难以成药的一些基因,而 且短序列的一些核酸药物通常是可以进行化学合成,制备相对简单一些,更容易 保证合成可得性和批次间稳定性。
作为核酸药物中的代表,小核酸药物展现了极大的潜力,包含反义寡核苷酸(ASO)、 小发卡 RNA(shRNA)、小干扰 RNA(siRNA)。小核酸药物从基因水平开始治疗, 相比蛋白药物有明显的优势。传统小分子化合物的发现过程中,先导化合物的发 现存在比较大的偶然性,而小核酸药物的最大优势是,只需要针对小核酸药物的 基因开发合适的序列,就可以开发成为新的药物,该途径避免了研发过程中的盲 目性。确定了小核酸药物的靶标序列后,其流程较快,且耗时明显更短,而且小 核酸药物的生物特异性也是非常高的。多年来,小核酸的化学修饰与递送系统改 进不仅增强了特异性和功效,而且减少了副作用。近年来,小核酸药物因其独特 的优势已成为治疗各种疾病的有前途的工具。

1.2 小核酸药物的发展现状
小核酸药物目前主要分为反义寡核酸药物(ASO)、RNA 干扰药物(siRNA,miRNA), 由于 miRNA 目前尚无获批药物,故本报告将集中于 ASO 与 siRNA 这两类小核酸药 物的分析。从获批情况上来看,自小核酸类第一个药物 Vitravene 上市以来,小核 酸行业已经历了 20 年的时间,迄今为止一共有 10 个 RNA 的药物上市,而且由于 行业技术以及监管的逐步成熟,近年来小核酸类药物的审批有了明显的加速。2015 年以前小核酸领域仅有 2 款药物上市,在 2018 年至今,已经先后有 6 款药 物上市。
目前,从治疗领域来看,小核酸药物研发的重点治疗领域包括杜氏肌营养不良、肿瘤、囊性纤维化等各类疾病。由于小核酸药物兼具基因修饰和传统药物的双重 特点,故未来将在多个领域大展身手,预计在基因遗传性疾病和病毒感染性疾病 领域中将有不俗表现。
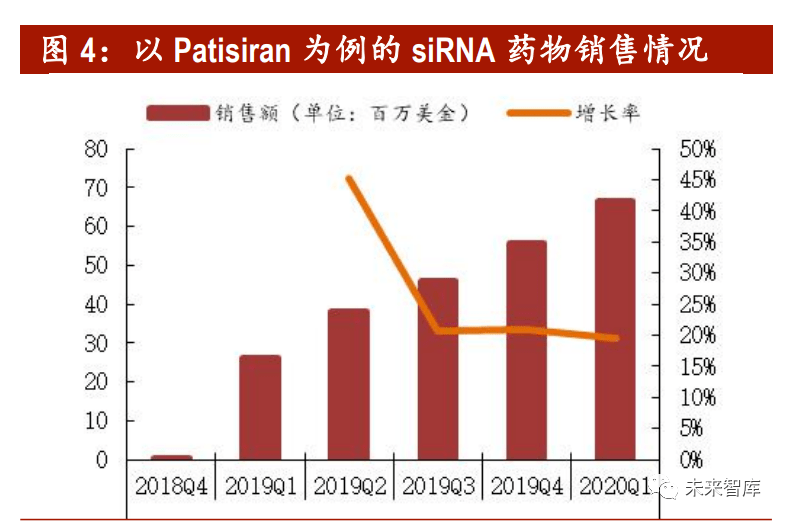
目前小核酸药物已有多款药物获批,并且在商业上取得了一定的成功。成功的代表药物是 ASO 药物 Nusinersen,用于治疗脊髓性肌萎缩症(SMA),截至 2019 年 底,其累计销售额为 47 亿美元;另外,目前批准的两种 siRNA 药物 Patisiran 和 Givosiran 也都取得了极好的销售额,Patisiran 在 2019 年上市的第一年销 售额已超过 1.5 亿美元。
2、 小核酸药物的作用机理与研发趋势
2.1 ASO 与 siRNA 药物作用机理(略)
2.2 ASO 与 siRNA 的管线研发现状
对于 ASO 药物,目前 ASO 药物全球研发尚处行业发展期,由于行业进入门槛较高, 全球实验室阶段后的项目不足 300 个,其治疗领域主要集中于肿瘤、神经与肌肉 疾病。就行业集中度而言,头部公司 Ionis、Sarepta、WAVElife 等公司均有较 长时间的积淀,行业集中度相对较高。这主要是因为 ASO 药物体积相对较小、亲 水性较低,有一定的通过胞饮直接进入细胞的能力,行业早期大多采用对 ASO 直 接化学修饰(降低递送效率以换取更简单的成药性)的方式进行药物改造,因而 更容易使得早期进入行业的企业形成专利。但是,近年来随着新型递送系统的出 现以及单纯化学修饰的 ASO 递送效率仍难以让人满意,一批以递送技术为切入点 的生物医药企业正在进入 ASO 领域。
对于 siRNA 药物,与 ASO 类似,目前 siRNA 药物全球研发尚处行业发展期,全球 实验室阶段后的项目大约 300 个,整体发展态势良好,其治疗领域主要集中于肿 瘤、神经与眼科。就行业集中度而言,头部公司 Alnylam、Dicerna、Arrowhead 等公司均有较长时间的积淀,行业集中度相对较高。由于 siRNA 分子量相较于 ASO 更大,且电荷性更强,siRNA 更难依靠自身进入细胞,所以 siRNA 药物对于 载体的要求更高,这也是为何 siRNA 药物获批相较于 ASO 药物更晚的一大原因。目前,siRNA 领域头部的企业都基于自身的技术特点,有自己或者授权引进了递 送平台,递送技术是生物医药企业进入 siRNA 领域的一大切入点。
2.3 小核酸药物化学修饰发展趋势
天然存在的小核酸具有较差的稳定性和非常低的特异性,并且在体内具有许多副 作用。化学修饰是增强小核苷酸药物递送的有效方法之一。磷酸骨架,核糖部分 和碱基本身的修饰已被广泛采用,以改善寡核苷酸药物的类药物性质,从而增强 递送。
具体而言,利用修饰来改善寡核苷酸的药代动力学,药效学和生物分布。对于某 些治疗方式的功能性,还需要特定的修饰方式。例如,2'-OMe 和硫代磷酸酯(PS) 修饰的组合促进了与胆固醇结合的 siRNA 的全身给药,并在体内实现了有效的基 因沉默,例如 2'-OMe 和 2'-F 的组合已用于 ONPATTRO;采用硫代磷酸酯(PS), 2'-OMe,2'-F 和 2'-deoxy 修饰的 inclisiran(ALN-PCSsc)亦被用于治疗高胆 固醇血症。目前,Alnylam,Arrowhead,Silence,Dicerna 等头部企业在自身 ASO 与 siRNA 管线成药性设计时都采用了多种化学修饰并用的方法以增加其药物 的成药性,并且随着对于核酸序列以及化学修饰认知的加深,对于核酸的化学修 饰也经历了从最早的不修饰到部分修饰,再到现在的全修饰。
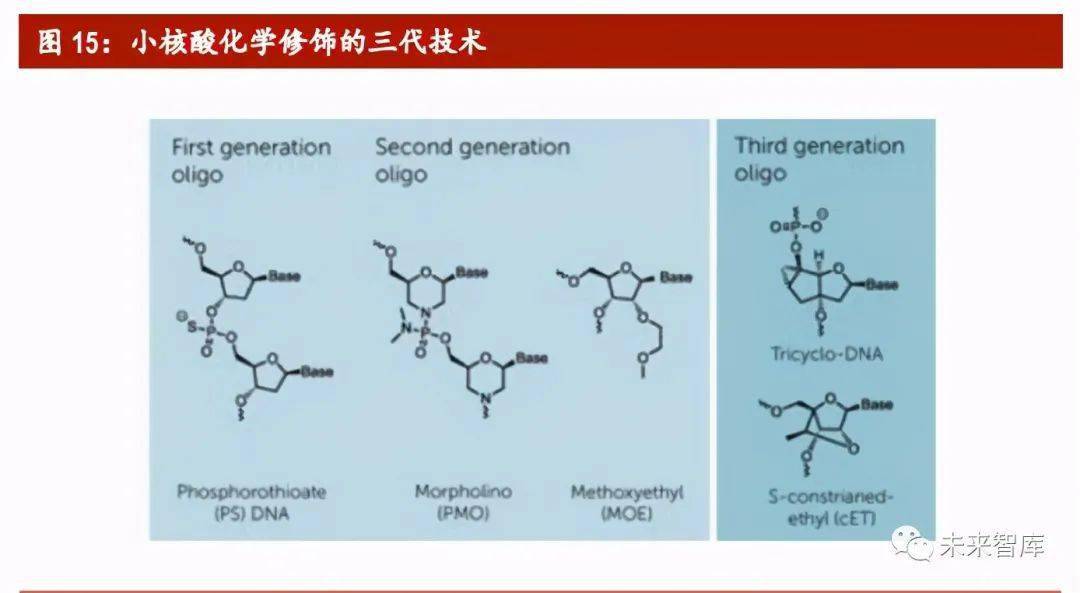
目前,对于核酸的化学修饰经过了数十年的发展,已经发展出了 3 代技术。最常 用的化学修饰是第一代的硫代磷酸酯和第二代的甲基膦酸酯。膦酸甲酯不带电, 因此比天然 DNA 或 RNA 更具亲脂性,并且可以更好地穿透细胞。但是,甲基膦 酸酯的溶解度一直是个问题,常与膜结合,仅有较少修饰后小核酸能进入细胞质 内。因此,后续又产生了第三代 PNA、LNA 等技术。但这些技术或多或少仍有潜 在的肝毒性以及效率低下等问题,工业界与学界也意识到,化学修饰对于小核酸 药物递送十分重要,但如靶向性等大量问题单纯依靠化学修饰还是难以解决,最 终还是需要依靠递送系统。

2.4 小核酸药物递送系统发展概况
目前针对 RNAi 给药,好的递送系统是解决挑战的重中之重,目前领先公司 Alnylam 获批的药物一款采用脂质体 LNP、一款采用 Galnac 递送系统。
3、 反义寡核苷酸(ASO)已上市及潜力药物分析(略)
目前全球上市的 ASO 药物一共有 8 个,这 8 个药物的作用机制也不完全一样。
3.1 Fomivirsen—开创 ASO 药物之先河
3.2 Mipomersen—降脂领域第一款 ASO 药物
3.3 Eteplisen—争议中前行的 ASO 药物
3.4 Nusinersen—第一款重磅炸弹
3.5 Inotersen—商业化上落于下风
3.6 Volanesoren—静待继续开花结果
3.7 Golodirsen 与 Viltolarsen—后续值得关注
3.8 ASO 成功的关键因素
总体来看,ASO 药物的商业化成功与否主要建立在两方面:1、对于疾病致病病 理的研究;2、本身的临床疗效。
在疾病致病病理的研究上,无论是 DMD51 号外显子还是 53 号外显子药物的出现, 还是针对 SMA 药物的出现,这些精妙的设计都是建立在对于疾病致病机理深入的 认知上,因此,未来 ASO 药物的蓬勃发展必然是伴随着疾病 Biology 的研究不断 深化,而近年来精准医学的发展正不断使得 Biology 研究加速。
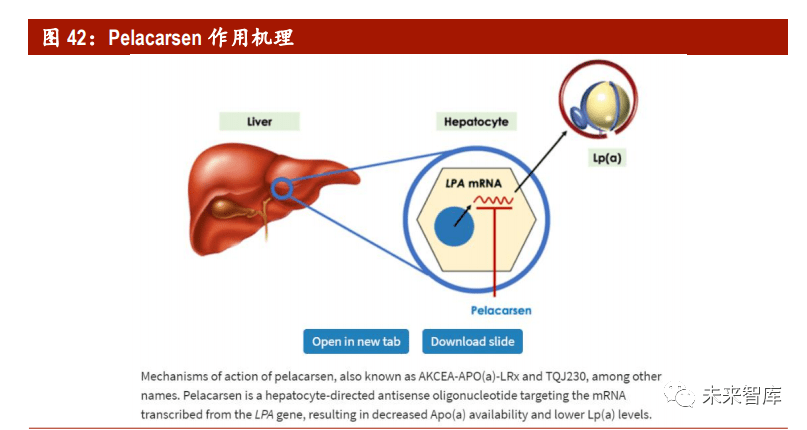
脂蛋白 a(Lp(a))是一种高度致动脉粥样硬化、类似 LDL 的脂蛋白,通过二硫 键连接到载脂蛋白 a(Apo(a)),Apo(a)由 LP(a)基因编码。Lp(a)具有 促炎、促动脉粥样硬化和血栓形成特性,并已通过流行病学研究证实与心肌梗塞、 中风和外周动脉疾病相关。LP(a)的水平在出生的时候就已经确定了,和后天 生活方式无关,目前已有的降低胆固醇的药物也没法控制,目前全球约有 800-1000 万人群 LP(a)表达异常。
Pelacarsen是用 GALnac 偶联的 ASO 药物,采用全 PS 骨架及 2’-MOE 修饰用来抑 制 Apoa 的 mRNA,从而 LP(a)的水平。
4、 siRNA 药物—每一部分都匠心独具
目前获批上市的 siRNA 药物有两款,分别为 Alnylam 治疗 haTTR 的 Patisiran 和 治疗急性肝卟啉症(AHP)的 Givosiran。由于与 ASO 药物相比,siRNA 药物由于 体积更大,且亲水性更强,较难直接通过细胞膜摄取,并且 siRNA 暴露血液会有 稳定性问题并造成免疫原性,因而无递送系统 siRNA 药物基本无法达到理想递送 水平。目前上市的两款 siRNA 药物主要采用的递送系统均为较成熟的递送技术脂 质体(LNP)与 GalNAc。
4.1 Patisiran-基于脂质体 LNP,实现 siRNA 药物零的突破
LNP 递送 siRNA 第一个成功上市的药物是 Alnylam 的 Patisiran。2018 年 8 月 FDA 批 准了 Alnylam 的 RNAi 药物 Onpattro (通用名 patisiran),用于治疗转甲状腺素蛋白淀 粉样变性(haTTR)引起的神经损伤。由于 haTTR 疾病分析已在先前 Inotersen 介 绍部分中进行了分析,在此就不赘述。作为第一个上市的 siRNA 药物,无论是核酸的修饰技术,还是递送系统的设计上,Patisiran 都可谓是反映了 Alnylam 数十年 技术的演进,每一个部分均可谓是匠心独具。
4.1.1 核酸的化学修饰
Patisiran 是化学合成的双链寡核苷酸。正义链和反义链各包含 21 个核苷酸。有义链的 19 个核苷酸与反义链的互补 19 个核苷酸杂交,从而形成 19 个核苷酸 碱基对,并在每条链上留下两个 3'-末端核苷酸作为未杂交的突出端,在修饰上 Patisiran 同时应用了 2’-O-M 和 2’-O-Me 修饰。并且 siRNA 的化学修饰相较 ASO也更为复杂,核酸修饰的顺序以及各类修饰所占比例也会影响最终药物的稳定性 与疗效。
Patisiran 作为较早开发的 siRNA 药物,采用的是部分核酸修饰的方式,尚未采 用 STC 与 ESC 修饰模板。从 Patisiran 到后续的药物如 revusiran(采用 STC) 和 Givosiran(采用 ESC)在 siRNA 的核酸修饰上,可以看到 Alnylam 多年来经 验积累与技术提升的过程。
从核酸修饰的演进过程上看,即使 Patisiran 没有采用最新的核酸修饰平台技术, 仍保证了较好的疗效,主要原因在于核酸的修饰本身可改进的空间并不大,主要 还是集中在提高稳定性、减毒增效上,与化学修饰相比,可能递送系统的提升更 为关键。
版权归属原作者所有!若涉及版权问题,敬请原作者联系我删除!